杭州医学院科研团队在《Molecular Cancer》发表研究成果
近日,杭州医学院梁广教授创新团队张衍梅课题组在国际TOP期刊《Molecular Cancer》杂志(中科院1区,IF=41)上发表研究论文《BTApep-TAT peptide inhibits ADP-ribosylation of BORIS to induce DNA damage in cancer》。该研究揭示了肿瘤组织中普遍表达的癌蛋白BORIS引导癌细胞发生异常DNA修复的分子机制,并首次报道了靶向抑制癌蛋白BORIS 功能的抑制肽BTApep-TAT。该论文第一单位是杭州医学院,共同第一作者分别为检验医学院(生物工程学院)的张衍梅和方梦蝶,共同通讯作者分别为张衍梅和梁广。
BORIS蛋白在几乎所有类型的肿瘤组织中表达,但相应正常组织中不表达。BORIS的存在亦导致肺癌、结直肠癌、脑癌等癌症的多药耐药性。BORIS的缺失或表达减低抑制癌细胞增殖以及癌症的发生发展,但分子机制不明。由于缺乏靶向BORIS的抑制物,长期阻碍了对BORIS功能的解析及其临床应用研究。
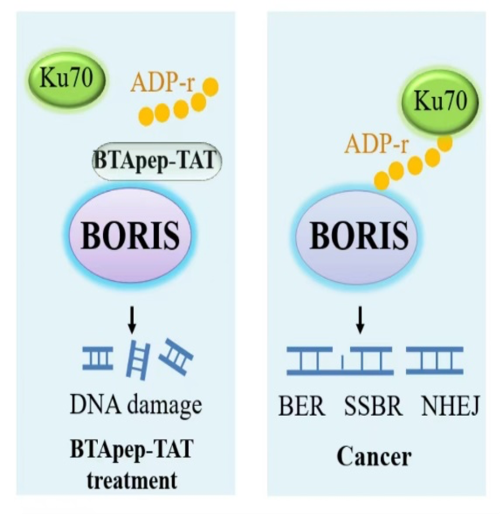
课题组经过努力,筛选出了特异性结合且抑制BORIS功能的多肽BTApep-TAT。BTApep-TAT结合BORIS的N端氨基酸,诱导癌细胞凋亡和DNA损伤,并缓解非小细胞肺癌的发生发展。在此基础上,课题组利用BTApep-TAT研究了BORIS对癌细胞DNA损伤修复的功能。课题组发现BORIS可促进癌细胞中的单链或双链DNA损伤修复,而BTApep-TAT对BORIS的抑制导致癌细胞DNA损伤。进一步研究发现,BORIS蛋白198-228AA区段内的核糖基化修饰响应癌细胞中DNA的损伤,BORIS的核糖基化募集Ku70参与修复细胞内的DNA的损伤。BORIS蛋白198-228AA区段内谷氨酸上的核糖基化是修复癌细胞中DNA损伤的关键原因。BTApep-TAT对BORIS 198-228AA区段内谷氨酸上核糖基化修饰的抑制是杀伤癌细胞的主要原因。
BORIS核糖基化修饰促进癌细胞DNA损伤修复的机制示意图
本研究首次发现了BORIS蛋白上的调控癌细胞DNA损伤修复功能的翻译后修饰的类型和关键氨基酸位点,解密癌蛋白BORIS在癌细胞中的作用机制;首次筛选获得靶向抑制BORIS功能的抑制肽,为临床上利用BORIS诊断癌症提供了依据,也为靶向BORIS的癌症治疗提供了前体药物和评价方法。
编辑 I 张衍梅 初审 I 应士波 终审 I 许秋然