Org Lett | 我校张逢质/张茜团队报道电化学驱动的镍催化亲电还原偶联反应:实现α-烯基酰胺的精准合成
发布时间:2025-06-02 16:22
浏览次数:
2024年7月23日,杭州医学院张逢质/张茜团队在国际权威期刊《Org. Lett.》(中科院一区,IF=4.9)上在线发表了题为“Electrochemical Nickel-Catalyzed Cross-Electrophile Coupling of Alkenyl Triflates with α‑Chloroamides”的研究论文。
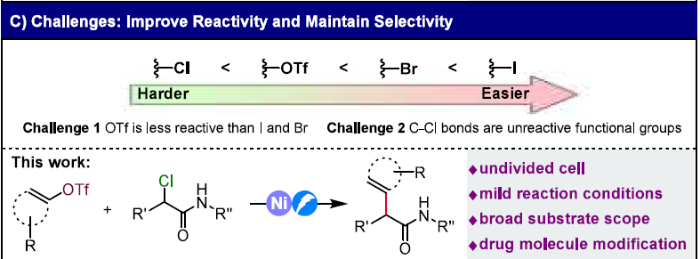
α-官能团化的酰胺衍生物是天然产物、药物活性成分及功能材料合成的关键中间体,但其空间位阻较大的结构难以通过传统方法高效构建。传统交叉偶联反应依赖对空气/水分敏感的有机金属试剂,官能团耐受性差且原子经济性低。近年来,电化学交叉亲电偶联(eXEC)因其绿色、高效的特点成为C–C键构建的新策略,但现有研究多局限于溴/碘代物,而氯代物与三氟甲磺酸酯的偶联仍具挑战性——因其氧化加成能垒高、易发生副反应。
图1. 电化学驱动镍催化亲电还原偶联反应
该工作首次实现了电化学镍催化烯基三氟甲磺酸酯与α-氯代酰胺的交叉偶联,突破传统卤代物限制,为α-功能化酰胺衍生物的绿色合成开辟新路径。
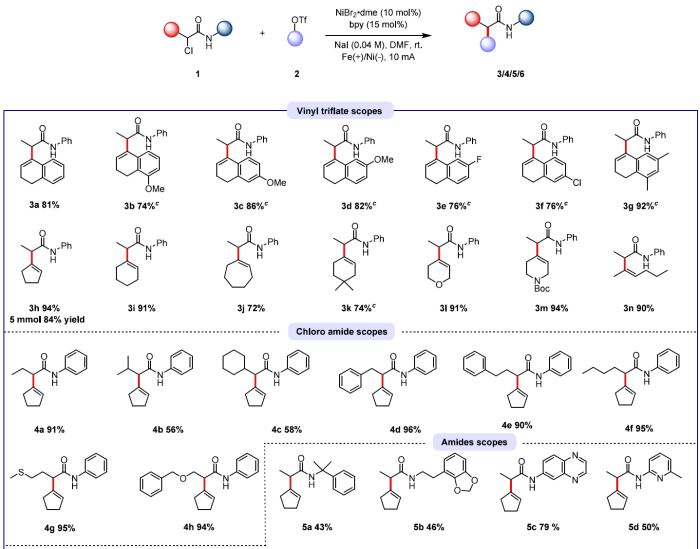
本论文所开发的方法具有极其广泛的底物兼容性。此外,本文成功实现了多个天然产物及药物的后期官能团化,所构筑的新型类药分子化合物库,为药物开发、生物活性筛选和成药性研究提供基础。
图2. 广谱的底物兼容性及药物分子合成实例
杭州医学院张茜讲师为本论文的第一作者,张逢质教授为通讯作者,论文第一通讯单位为杭州医学院。相关工作得到了国家自然科学基金和杭州医学院求真人才启动经费等的支持。
原文链接:https://pubs.acs.org/doi/abs/10.1021/acs.orglett.4c02072
来源:叶增辉 审核:科研处