AS | 杭州医学院许秋然团队构建工程菌复合系统实现STING通路介导肿瘤免疫治疗
近日,杭州医学院许秋然研究员课题组联合华中科技大学等在国际权威期刊《Advanced Science》(中科院TOP一区,影响因子IF=14.1)发表题为“Engineered Bacteria Factory Integrating Drug Delivery and Antibody Manufacture for Activating the STING Signal Pathway Mediated Tumor Immunotherapy”的研究型论文。该研究创新性构建“缺氧响应工程菌-脂质体”复合递送治疗系统(HRB@LC),成功实现肿瘤部位免疫检查点抑制剂的原位合成与STING信号通路的精准激活,二者协同作用显著增强机体全身抗肿瘤免疫应答,为肿瘤免疫治疗领域提供具有良好临床转化前景的新型递送与治疗技术平台。
在肿瘤免疫治疗领域,巨噬细胞作为固有免疫系统的核心功能组分,具备快速免疫应答、无需依赖肿瘤抗原识别等独特优势,是肿瘤免疫治疗的重要潜在靶点。然而,肿瘤细胞异常高表达的CD47分子可通过与巨噬细胞表面SIRPα受体特异性结合,传递免疫抑制信号,进而介导肿瘤细胞免疫逃逸;与此同时,STING激动剂虽可有效激活巨噬细胞固有免疫应答,改善肿瘤局部免疫抑制微环境,但该类分子存在亲水性强、胞质递送效率低下、体内易被降解清除等技术瓶颈,限制其临床应用效果。传统免疫检查点抑制剂(如CD47抗体)临床应用中存在脱靶效应引发的全身毒性反应、体内易降解导致的治疗效能不足等问题,现有递送系统难以实现免疫检查点抑制剂的原位持续合成与STING激动剂靶向递送的协同调控,严重制约肿瘤免疫治疗的进一步提升。因此,突破递送系统技术瓶颈,实现肿瘤免疫逃逸阻断与固有免疫应答激活的协同调控,是当前肿瘤免疫治疗领域亟待解决的关键科学问题。
针对上述关键科学问题,研究团队基于合成生物学与材料工程学交叉融合技术,设计并构建“工程菌原位合成-脂质体靶向递送”协同治疗策略。以减毒大肠杆菌MG1655为宿主载体,将含缺氧启动子fdhF(PfdhF)及pelB-CD47抗体(aCD47)编码序列的可重编程质粒定向转入宿主菌,成功构建缺氧响应型工程菌(HRB),该工程菌可在肿瘤组织缺氧微环境中特异性启动aCD47的表达与分泌;同时,采用薄膜水合法制备负载STING激动剂cGAMP的pH响应性脂质体(LC),其亲水内核可高效包裹cGAMP,表面修饰醛基官能团后,通过席夫碱反应与HRB表面氨基实现共价结合,最终构建形成HRB@LC复合系统。该复合系统通过双重微环境响应机制实现肿瘤精准治疗:HRB响应肿瘤组织缺氧微环境,特异性表达并分泌aCD47,高效阻断CD47-SIRPα信号通路介导的肿瘤免疫逃逸;LC响应肿瘤局部弱酸性微环境,从HRB表面解离脱落,被巨噬细胞吞噬后定向释放cGAMP,激活STING信号通路,进而协同诱导巨噬细胞M1型极化、树突状细胞成熟及细胞毒性T细胞浸润与活化。
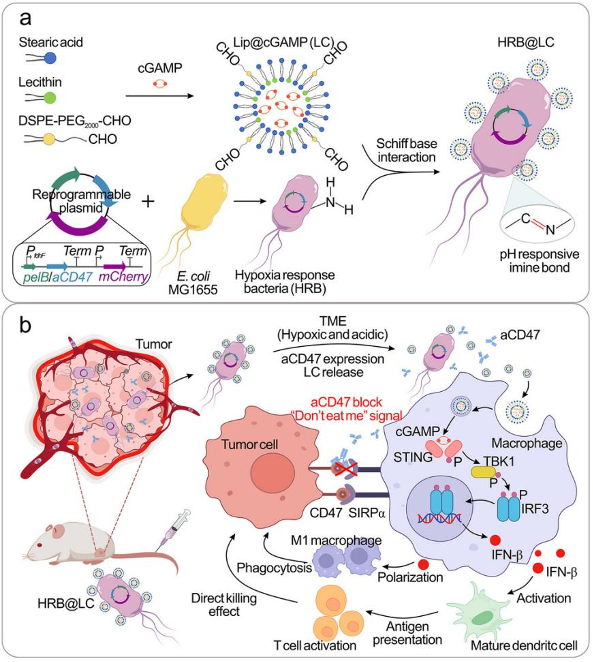
图形摘要:HRB@LC的合成及其抗肿瘤机制。(a)HRB@LC制备过程示意图。(b)表达免疫检查点抑制剂的工程菌与载有cGAMP的脂质体相结合,用于将药物递送至肿瘤区域,增强抗肿瘤免疫治疗的示意图。
该研究通过合成生物学与材料工程的交叉创新,建立工程菌“活体工厂”与脂质体递送系统的协同治疗,突破传统肿瘤免疫治疗的多重瓶颈:HRB实现免疫检查点抑制剂的肿瘤原位持续合成,降低脱靶毒性并提升疗效;LC有效解决STING激动剂递送难题,增强胞质递送效率;二者协同作用实现免疫逃逸阻断与固有免疫激活的双重效果,显著提升全身抗肿瘤免疫应答。这种集原位合成、靶向递送、多机制协同治疗于一体的新型平台,不仅为乳腺癌等实体瘤提供创新治疗方案,也为其他恶性肿瘤的免疫治疗开辟新路径,具有重要的临床转化价值。
许秋然研究员为论文的末位通讯作者,论文通讯单位为杭州医学院,华中科技大学赵元弟教授、樊锦轩等为论文共同通讯作者。
文献来源:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202518172
图/文来源:许秋然 审核:科研处、人文社科处