Nat. Commun. | 我校许秋然团队阐明导电聚合物稳定性纳米酶抑制铁蓄积和脂质过氧化治疗脓毒症心肌损伤
近日,杭州医学院许秋然研究员课题组联合中国科学院生物物理研究所、郑州大学等在国际权威期刊《Nature Communications》(中科院TOP一区,影响因子IF=15.7)发表题为“Conducting polymer-stabilized nanozymes alleviate sepsis-induced myocardial injury by inhibiting iron accumulation and lipid peroxidation”的研究性论文。通讯作者为杭州医学院许秋然研究员、中国科学院生物物理研究所范克龙研究员及郑州大学姜伟教授。
01研究背景
脓毒症是一种由机体对感染反应失调引起的全身性炎症反应和器官功能障碍综合征,可引起全身器官衰竭。脓毒症心肌损伤(Septic cardiomyopathy, SC)是脓毒症常见的并发症之一,以左心室和(或)右心室收缩和舒张功能障碍、左心室输出量下降、射血分数降低为主要病理特征。近年来的研究表明,心肌细胞内严重的氧化应激、铁蓄积以及随之而来的脂质过氧化——即铁死亡(Ferroptosis)过程,在脓毒症心肌损伤的发生发展中扮演着关键角色。
纳米酶作为一种具有类天然酶催化活性的纳米材料,因其优异的理化稳定性和可调控的催化活性,在调节微环境氧化还原稳态方面展现出巨大的潜力。然而,如何进一步提高纳米酶在复杂生理环境中的稳定性和催化活性,并实现对心肌细胞氧化应激与铁代谢的高效双重调控,仍是该领域面临的重要挑战。
针对这一难题,杭州医学院许秋然研究员与中国科学院生物物理研究所范克龙研究员、郑州大学姜伟教授团队联合攻关,巧妙地设计并开发了一种新型导电聚合物稳定性纳米酶(PPy-co-PTh stabilized Ruzymes)。该纳米酶不仅具备高效的抗氧化类酶活性,还能精准抑制心肌细胞内的铁蓄积与脂质过氧化,从而显著缓解脓毒症诱发的心肌损伤。
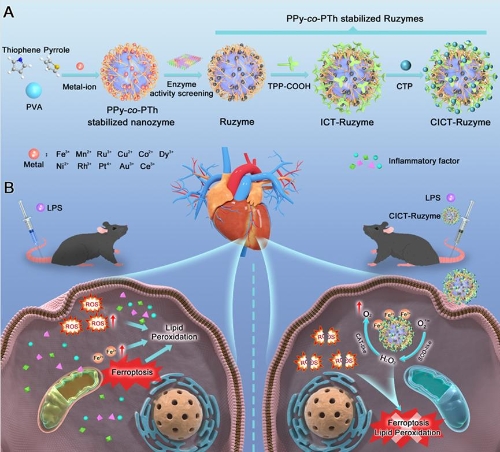
图1. PPy-co-PTh stabilized Ruzymes的合成路线及其缓解脓毒症心肌损伤的机制示意图
02研究内容
研究团队首先通过精准的化学合成策略,构建了导电聚合物纳米酶。导电聚合物不仅赋予了该纳米颗粒优异的生物相容性和胶体稳定性,其独特的共轭骨架更使其具备了优良的导电性。相较于非聚合物纳米酶,该种纳米酶在模拟生理环境下展现出更强的活性氧清除能力,发挥其类过氧化氢酶活性,持续清除H2O2分解,并在过量H2O2环境中能够防止自身过度氧化,维持自身的稳定性。另外,这种导电聚合物纳米酶还具备良好的含氮自由基清除能力和铁螯合性能。
为了探究该纳米酶在细胞层面的保护机制,研究人员构建了体外心肌细胞氧化应激模型。研究表明,该导电聚合物纳米酶能够被内化进入心肌细胞,通过发挥其抗氧化类酶活性清除活性氧,并螯合Fe2+,从而有效抑制铁积累和脂质过氧化,缓解氧化应激。
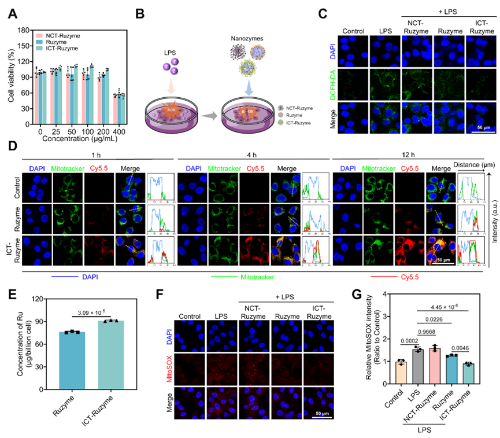
图2. 体外评估PPy-co-PTh stabilized Ruzymes 对心肌细胞内ROS的清除作用
为了评估导电聚合物纳米酶的体内治疗效果,使用脂多糖建立了 SC 小鼠模型。通过静脉注射,经过心脏靶向肽修饰的导电聚合物纳米酶能够有效富集于受损的心肌组织中。超声心动图、组织病理学以及血清学生化指标的系统评估表明,与非聚合物纳米酶相比,导电聚合物纳米酶能够有效缓解心肌组织的病理变化,改善心功能。
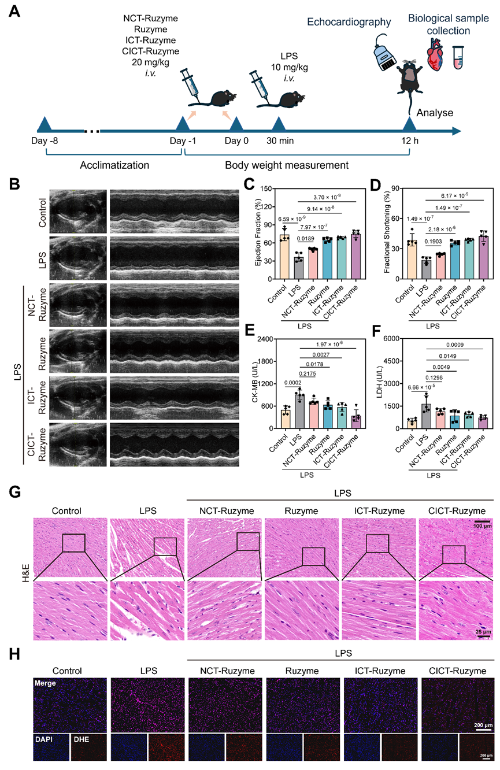
图3. PPy-co-PTh stabilized Ruzymes对SC小鼠的治疗效果
03总结与展望
综上,研究提出了一种基于导电聚合物调控纳米酶催化活性与稳定性的创新策略。该研究不仅证实了这种新型纳米酶能够有效干预氧化应激状态下心肌细胞的铁蓄积与脂质过氧化进程,揭示了其在抗氧化应激和抑制铁死亡方面的深层机制,更为脓毒症心肌损伤以及其他与氧化应激失衡相关的危重症心血管疾病提供了一种安全、高效且具有一定转化前景的纳米医学治疗新范式。随着多功能纳米酶设计的不断优化,未来此类材料有望在重症急救与个体化治疗中发挥更重要的作用。
图文:许秋然团队
审核:银国利
终审:许秋然